
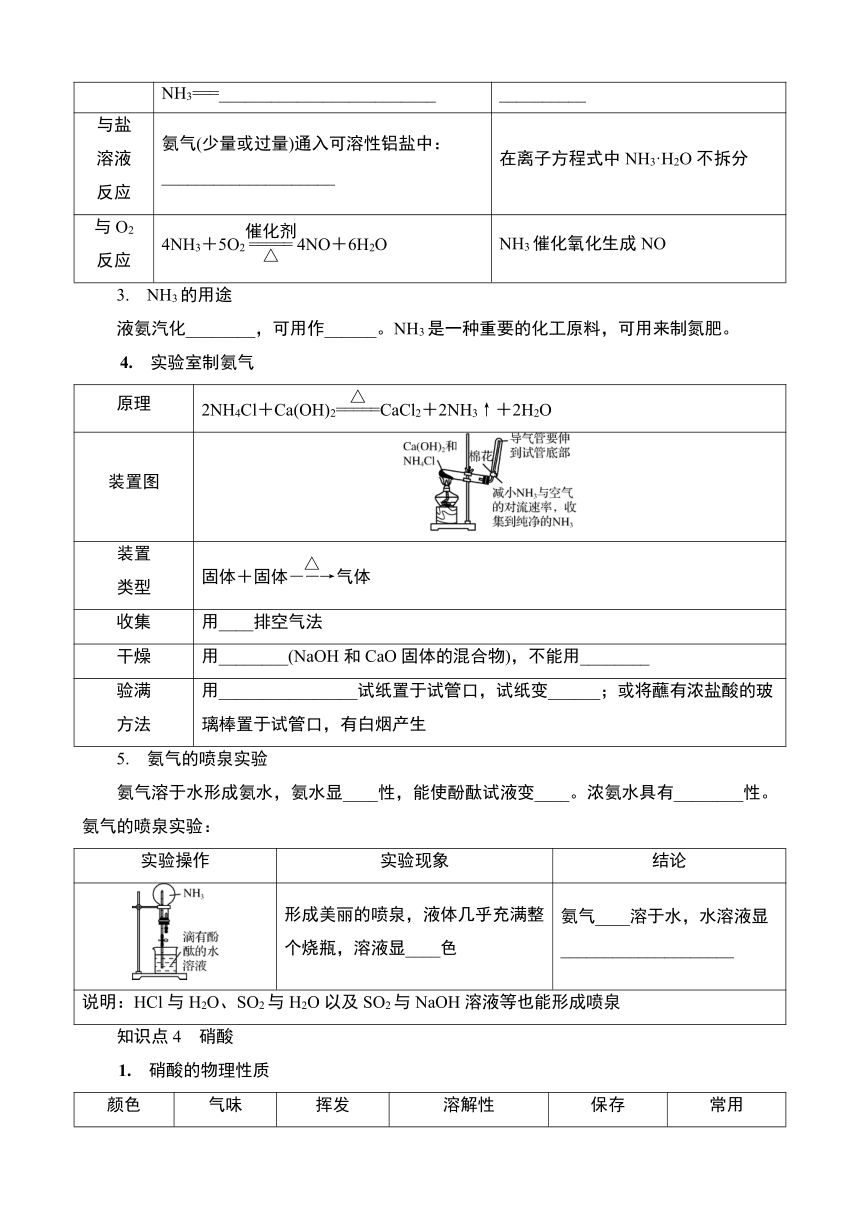
课时10 氮及其化合物 知 识 梳 理 知识点1 氮气性质 1. 氮气的物理性质 颜色、状态 气味 在水中溶解性 无色气体 _____ _____ 2. 氮气的化学性质 知识点2 NO和NO2的比较 NO NO2 物理性质 颜色 无色 红棕色 溶解性 不溶于水 能溶于水 收集方法 _____(不能用排空气法收集) _____ 化学性质 毒性 有毒 有毒 与O2反应 2NO+O2===2NO2 不反应 与H2O反应 不反应 3NO2+H2O===2HNO3+NO 知识点3 氨气 1. 氨气的分子结构与物理性质 电子式 密度 熔、沸点 颜色、气味 水溶性 _____ 比空气__ ____,易____ ____色、有_____气味 _____溶于水,1体积的水溶解约____体积的氨气 2. 氨气的化学性质 性质 化学(或离子)方程式 说明 与水反应 NH3+H2O??NH3·H2O??NH+OH- 计算氨水浓度时通常将____视作溶质 与酸反应 HCl+NH3===_____HNO3+NH3===_____ 蘸有浓氨水的玻璃棒与蘸有_____(或浓硝酸)的玻璃棒靠近,_____ 与盐溶液反应 氨气(少量或过量)通入可溶性铝盐中:_____ 在离子方程式中NH3·H2O不拆分 与O2反应 4NH3+5O24NO+6H2O NH3催化氧化生成NO 3. NH3的用途 液氨汽化_____,可用作_____。NH3是一种重要的化工原料,可用来制氮肥。 4. 实验室制氨气 原理 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O 装置图 装置类型 固体+固体气体 收集 用____排空气法 干燥 用_____(NaOH和CaO固体的混合物),不能用_____ 验满方法 用_____试纸置于试管口,试纸变_____;或将蘸有浓盐酸的玻璃棒置于试管口,有白烟产生 5. 氨气的喷泉实验 氨气溶于水形成氨水,氨水显____性,能使酚酞试液变____。浓氨水具有_____性。氨气的喷泉实验: 实验操作 实验现象 结论 形成美丽的喷泉,液体几乎充满整个烧瓶,溶液显____色 氨气____溶于水,水溶液显_____ 说明:HCl与H2O、SO2与H2O以及SO2与NaOH溶液等也能形成喷泉 知识点4 硝酸 1. 硝酸的物理性质 颜色 气味 挥发性 溶解性 保存 常用浓硝酸 ____色 有_____气味 ____挥发 能与水以_____混溶 ____色试剂瓶 质量分数为69% 2. 硝酸的化学性质 (1) 强酸性:具有酸的通性。 (2) 不稳定性:4HNO3_____ (生成的NO2溶解在浓硝酸中使溶液呈黄色)。 (3) 强氧化性: ①3Cu+8HNO3(稀)===_____ _____; ②Cu+4HNO3(浓)===_____ _____; ③C+4HNO3(浓)===_____ _____; ④钝化反应:常温下镁、铝、铁遇浓硝酸发生钝化。 知识点5 铵盐的性质 1. 铵盐 (1) 概念:由_____和_____形成的离子化合物。 (2) 物理性质:多为无色、易溶于水的晶体。 (3) 化学性质 ①不稳定性 a. NH4Cl受热分解:_____。 b. NH4HCO3受热分解:_____。 ②与碱反应 铵盐与碱溶液反应的离子方程式: a. 在稀溶液中不加热: NH+OH-===NH3·H2O b. 加热时或在浓溶液中:_____。 2. 铵根离子的检验 NH的检验原理:NH与OH-在加热条件下反应放出NH3,通过检验NH3,从而验证NH。 典 型 例 题 类型1 氮循环 (2022·江苏学测)自然界存在多种元素的循环,如图表示的是自然界中的( ) A. 碳循环 B. 氮循环 C. 氧循环 D. 硫循环 (2023·南京学测合格考)下列有关自然界中氮循环的说法错误的是( ) A. 工业合成氨属于人工固氮 B. 豆科植物可实现生物固氮 C. 含氮无机物与有机氮可以相互转化 D. 氨和铵盐在硝化细菌作用下被还原 类型2 氮的氧化物与酸雨 下列气体排放到空气中,不会导致酸雨的是( ) A. NO B. NO2 C. CO2 D. SO2 (2024·淮安合格考模拟二)下列关于二氧化氮的说法不正确的是( ) A. 是红棕色气体 B. 属于非金属氧化物 C. 能与水反应 D. 常温下易与氧气反应 类型3 氨气的性质 (2024·淮安合格考模拟)通入水中所得溶液呈碱性的气体是( ) A. NH3 B. NO2 C. SO2 D. HCl (2023·江苏部分重点中学学测合格考)如图为氨气溶于水 ... ...
~~ 已预览到文档结尾了 ~~