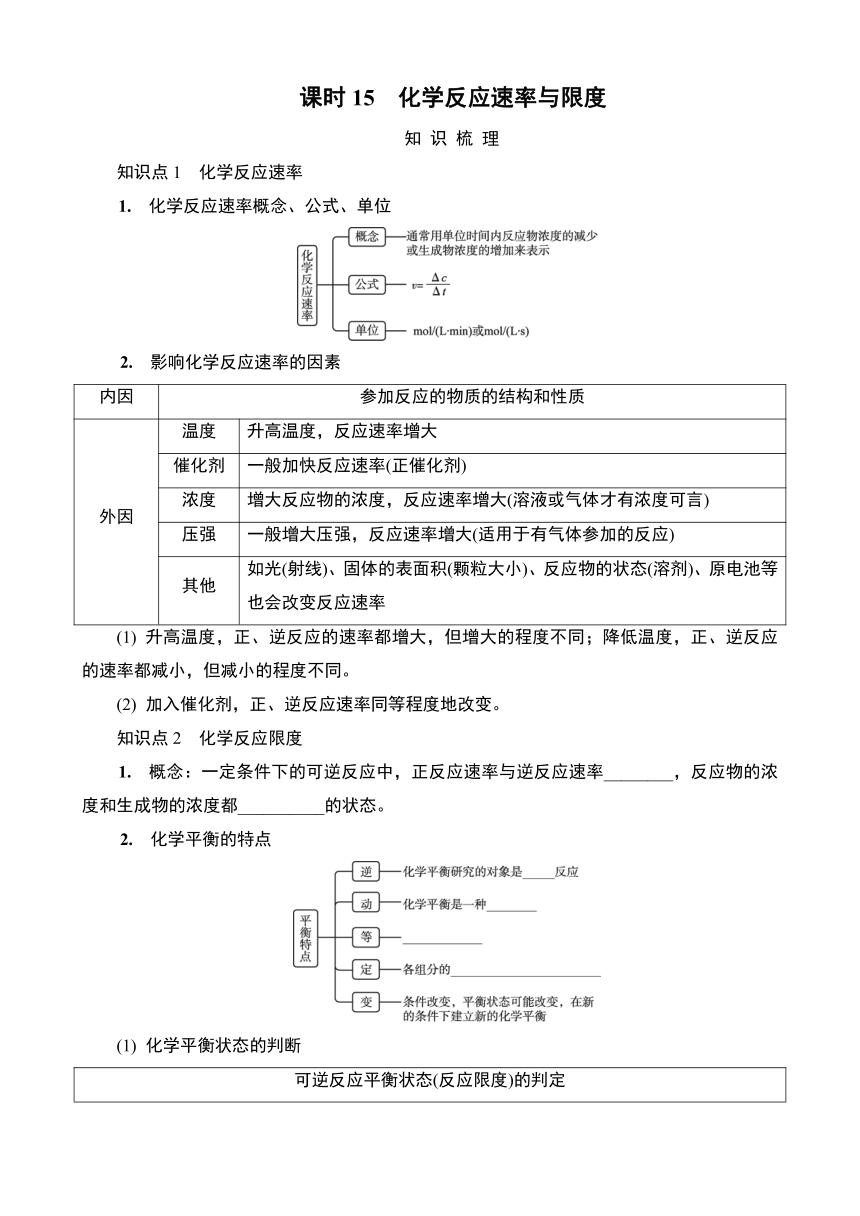

课时15 化学反应速率与限度 知 识 梳 理 知识点1 化学反应速率 1. 化学反应速率概念、公式、单位 2. 影响化学反应速率的因素 内因 参加反应的物质的结构和性质 外因 温度 升高温度,反应速率增大 催化剂 一般加快反应速率(正催化剂) 浓度 增大反应物的浓度,反应速率增大(溶液或气体才有浓度可言) 压强 一般增大压强,反应速率增大(适用于有气体参加的反应) 其他 如光(射线)、固体的表面积(颗粒大小)、反应物的状态(溶剂)、原电池等也会改变反应速率 (1) 升高温度,正、逆反应的速率都增大,但增大的程度不同;降低温度,正、逆反应的速率都减小,但减小的程度不同。 (2) 加入催化剂,正、逆反应速率同等程度地改变。 知识点2 化学反应限度 1. 概念:一定条件下的可逆反应中,正反应速率与逆反应速率_____,反应物的浓度和生成物的浓度都_____的状态。 2. 化学平衡的特点 (1) 化学平衡状态的判断 可逆反应平衡状态(反应限度)的判定 反应速率 v(正)=v(逆)≠0 浓度 各组分的浓度不再改变,不要求浓度之比等于化学计量数之比 百分含量 混合体系中,各组分的百分含量不再改变 颜色 对于有颜色的物质参加或生成的可逆反应,颜色不随时间发生变化 化学键 对同一物质而言,单位时间内,断裂化学键的物质的量与形成化学键的物质的量相等 (2) 有关反应速率、平衡状态的正误判断 已知反应:2SO2(g)+O2(g)2SO3(g), 按n(SO2)∶n(O2)=2∶1进行反应 改变条件 正误 解释 升高温度,正反应速率增大,逆反应速率减小 ——— 正、逆反应速率都增大 降低温度,加快反应速率 ——— 降低温度,反应速率减小 c(SO2)∶c(O2)∶c(SO3)=2∶1∶2,反应达到平衡 ——— 各组分浓度不变才是平衡状态 经充分反应,SO2的转化率为100% ——— 可逆反应中,反应物不能完全转化 加入合适的催化剂能够加快反应速率 ——— 加入合适的催化剂可加快反应速率 典 型 例 题 (2022·盐城学测合格考)工业上H2可以发生反应:CO+2H2CH3OH。下列有关说法不正确的是( ) A. 增大H2的浓度,可加快反应速率 B. 使用合适催化剂,可加快反应速率 C. 达到平衡时,正反应速率与逆反应速率相等 D. 达到平衡时,CO可以完全转化 (2022·江苏学测)甲醇与水蒸气制取氢气的反应为CH3OH(g)+H2O(g)CO2(g)+3H2(g),正反应是吸热反应。下列说法正确的是( ) A. 如图表示正反应过程的能量变化 B. 使用合适的催化剂能增大反应速率 C. 减小CH3OH的浓度能增大反应速率 D. 达到化学平衡时,CH3OH能完全转化为生成物 (2021·江苏学测)水-碳催化制氢的反应为C+H2OH2+CO。下列说法正确的是( ) A. 增大压强能减慢化学反应速率 B. 使用合适的催化剂能加快化学反应速率 C. 增大水蒸气的浓度能减慢化学反应速率 D. 达到化学平衡时,H2O全部转化为H2 (2020·江苏学测)反应2NO+2CON2+2CO2可应用于汽车尾气的净化。下列说法正确的是( ) A. 升高温度能减慢反应速率 B. 减小CO浓度能加快反应速率 C. 使用恰当的催化剂能加快反应速率 D. 达到化学平衡时,NO能100%转化为产物 (2024·扬州合格考模拟)反应2CO2+6H2??CH3OCH3+3H2O可用于CO2的资源化。下列关于该反应的说法正确的是( ) A. 升高温度能减慢反应速率 B. 减小CO2浓度能加快反应速率 C. 使用恰当的催化剂能加快反应速率 D. 达到化学平衡时,CO2能100%转化为产物 (2024·无锡合格考模拟)舍勒发现氯气是在1774年,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体,发生反应的化学方程式为MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O。下列反应条件的改变对实验室制备氯气速率的影响正确的是( ) A. 增大盐酸的浓度能加快反应速率 B. 若用稀盐酸与二氧化锰反应,则反应速率较慢 C. 升高温度能减慢反应速率 D ... ...
~~ 已预览到文档结尾了 ~~