
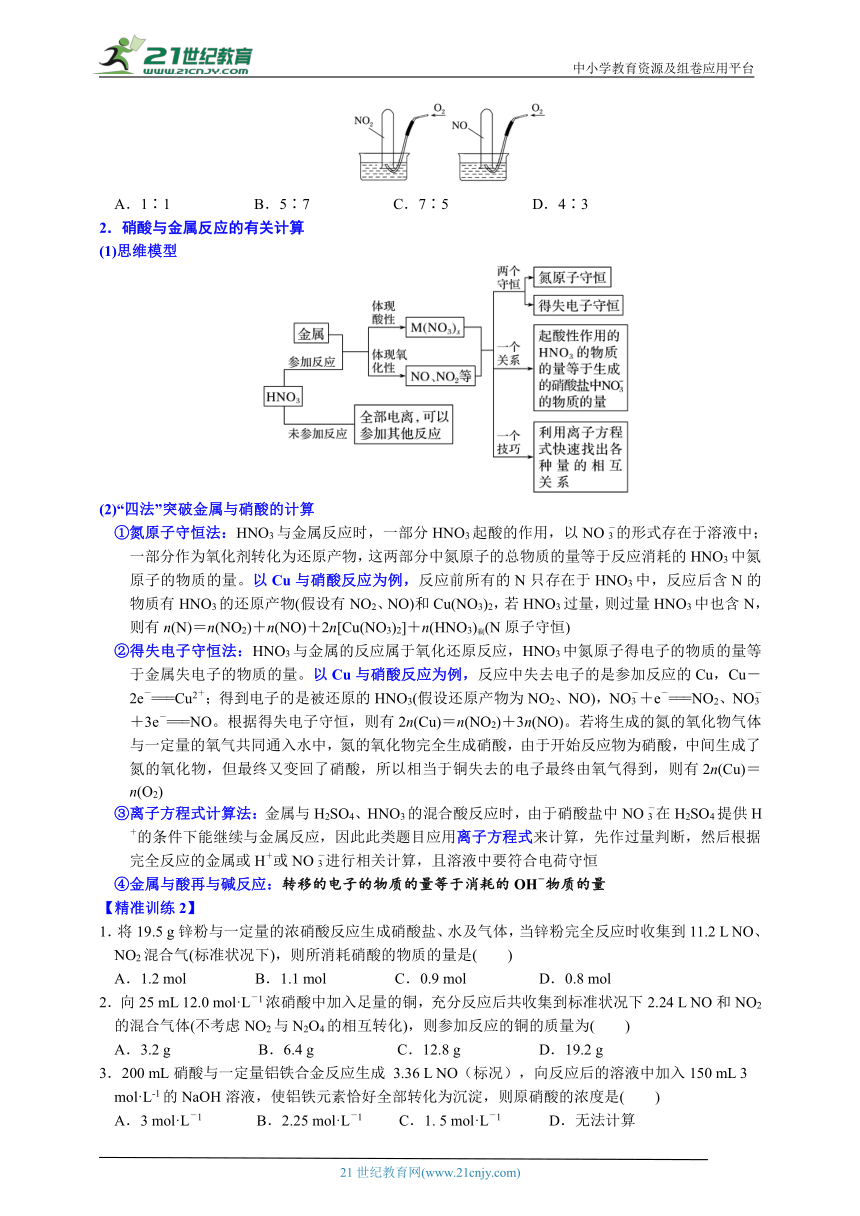
中小学教育资源及组卷应用平台 氮的氧化物的计算与硝酸相关的计算 【方法与规律】 1.氮的氧化物和O2、H2O反应的计算方法 (1)NO2和O2混合气体溶于水的计算 ①计算依据:3NO2+H2O===2HNO3+NO……………………i 2NO+O2===2NO2………………………………ii i×2+ii得:4NO2+O2+2H2O===4HNO3…………………iii ②由4NO2+O2+2H2O===4HNO3可知 V(NO2)∶V(O2) (2)NO与O2同时通入水中的计算 ①计算依据:2NO+O2===2NO2………………………………i 3NO2+H2O===2HNO3+NO……………………ii i×2+ii得:4NO+3O2+2H2O===4HNO3…………………iii ②由4NO+3O2+2H2O===4HNO3可知 V(NO)∶V(O2) (3)NO2、NO、O2三种混合气体通入水中 ①计算依据:3NO2+H2O===2HNO3+NO 4NO+3O2+2H2O===4HNO3 ②处理方法:将NO2与水先反应,按反应3NO2+H2O===2HNO3+NO,求出生成NO的体积,再加上原混合气体中NO的体积,得NO的总体积,最后按反应4NO+3O2+2H2O===4HNO3 进行计算 【精准训练1】 1.在一定条件下,将NO2和O2的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同温同压下),则原混合气体中氧气的体积为( ) ①1.2 mL ②2.4 mL ③3 mL ④4 mL A.①② B.②③ C.③④ D.①④ 2.60 mL NO2和O2的混合气体通入倒立在水槽中盛满水的玻璃筒(带刻度)中,充分反应后,筒内剩余10 mL气体,则原混合气体中的NO2与O2的体积比可能为( ) A.3∶1 B.6∶1 C.9∶1 D.12∶1 3.将充有m mL NO2和n mL NO气体的试管倒立于盛水的水槽中,然后通入n mL O2,且m>n,则充分反应后,试管中气体在同温同压下的体积为( ) A. mL B. mL C. mL D. mL 4.如图所示,相同条件下,两个容积相同的试管分别装满NO2和NO气体,分别倒置于水槽中,然后通过导管缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内充满液体。假设试管内的溶质不向水槽中扩散,则两个试管内溶液中溶质的物质的量浓度之比为( ) A.1∶1 B.5∶7 C.7∶5 D.4∶3 2.硝酸与金属反应的有关计算 (1)思维模型 (2)“四法”突破金属与硝酸的计算 ①氮原子守恒法:HNO3与金属反应时,一部分HNO3起酸的作用,以NO的形式存在于溶液中;一部分作为氧化剂转化为还原产物,这两部分中氮原子的总物质的量等于反应消耗的HNO3中氮原子的物质的量。以Cu与硝酸反应为例,反应前所有的N只存在于HNO3中,反应后含N的物质有HNO3的还原产物(假设有NO2、NO)和Cu(NO3)2,若HNO3过量,则过量HNO3中也含N,则有n(N)=n(NO2)+n(NO)+2n[Cu(NO3)2]+n(HNO3)剩(N原子守恒) ②得失电子守恒法:HNO3与金属的反应属于氧化还原反应,HNO3中氮原子得电子的物质的量等于金属失电子的物质的量。以Cu与硝酸反应为例,反应中失去电子的是参加反应的Cu,Cu-2e-===Cu2+;得到电子的是被还原的HNO3(假设还原产物为NO2、NO),NO+e-===NO2、NO+3e-===NO。根据得失电子守恒,则有2n(Cu)=n(NO2)+3n(NO)。若将生成的氮的氧化物气体与一定量的氧气共同通入水中,氮的氧化物完全生成硝酸,由于开始反应物为硝酸,中间生成了氮的氧化物,但最终又变回了硝酸,所以相当于铜失去的电子最终由氧气得到,则有2n(Cu)=n(O2) ③离子方程式计算法:金属与H2SO4、HNO3的混合酸反应时,由于硝酸盐中NO在H2SO4提供H+的条件下能继续与金属反应,因此此类题目应用离子方程式来计算,先作过量判断,然后根据完全反应的金属或H+或NO进行相关计算,且溶液中要符合电荷守恒 ④金属与酸再与碱反应:转移的电子的物质的量等于消耗的OH-物质的量 【精准训练2】 1.将19.5 g锌粉与一定量的浓硝酸反应生成硝酸盐、水及气体,当锌粉完全反应时收集到11.2 L NO、NO2混合气(标准状况下),则所消耗硝酸的物质的量是( ) A ... ...
~~ 已预览到文档结尾了 ~~