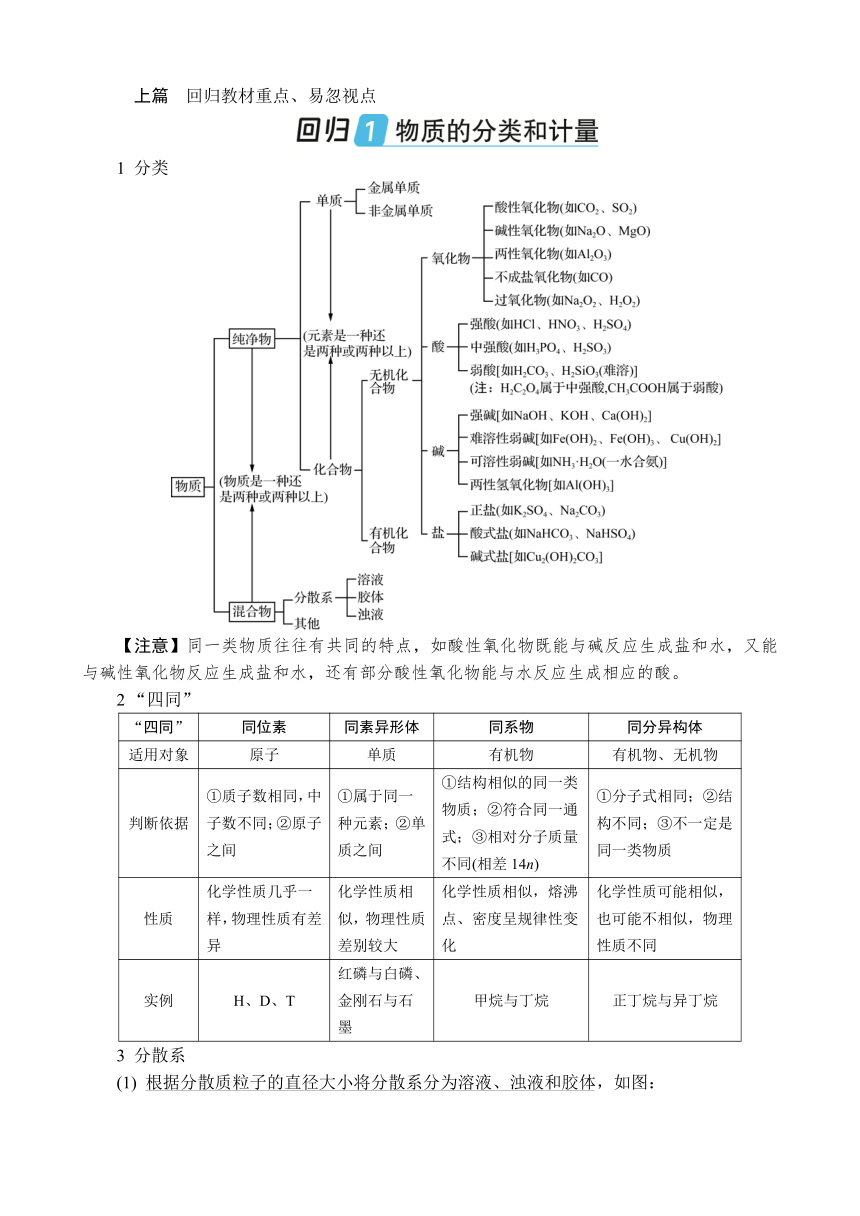

上篇 回归教材重点、易忽视点 1 分类 【注意】同一类物质往往有共同的特点,如酸性氧化物既能与碱反应生成盐和水,又能与碱性氧化物反应生成盐和水,还有部分酸性氧化物能与水反应生成相应的酸。 2 “四同” “四同” 同位素 同素异形体 同系物 同分异构体 适用对象 原子 单质 有机物 有机物、无机物 判断依据 ①质子数相同,中子数不同;②原子之间 ①属于同一种元素;②单质之间 ①结构相似的同一类物质;②符合同一通式;③相对分子质量不同(相差14n) ①分子式相同;②结构不同;③不一定是同一类物质 性质 化学性质几乎一样,物理性质有差异 化学性质相似,物理性质差别较大 化学性质相似,熔沸点、密度呈规律性变化 化学性质可能相似,也可能不相似,物理性质不同 实例 H、D、T 红磷与白磷、金刚石与石墨 甲烷与丁烷 正丁烷与异丁烷 3 分散系 (1) 根据分散质粒子的直径大小将分散系分为溶液、浊液和胶体,如图: (2) 胶体的性质及应用 ①性质 丁达尔效应:当光束通过胶体时,可以看到一条光亮的“通路”,该现象称为丁达尔效应。利用丁达尔效应可以鉴别胶体和溶液。 【提示】胶体的实质是分散质粒子的直径大小为1~100 nm;特征为丁达尔效应。 吸附性:能吸附水中的悬浮颗粒物并沉降。 【提示】胶体吸附性往往是由于具有很大的接触面积及胶体粒子带有一定的电荷。 ②明矾[KAl(SO4)2·12H2O]净水: Al3++3H2O===Al(OH)3(胶体)+3H+ Fe(OH)3胶体的制备: 向沸水中逐滴加入5~6滴饱和FeCl3溶液,继续煮沸至液体呈红褐色,停止加热。所得的液体就是Fe(OH)3胶体。 4 物质的量 (1) 物质的量 ①物质的量的符号为n,单位为mol。 ②阿伏加德罗常数:1 mol任何粒子所含的粒子数,符号为NA,通常用6.02×1023 mol-1表示。 ③N=nNA。 (2) 摩尔质量 ①单位物质的量的物质具有的质量。符号为M,单位为g/mol。 ②M=。 ③当质量以克为单位时,摩尔质量在数值上等于该物质的相对原子质量或相对分子质量。 (3) 气体摩尔体积 ①单位物质的量的气体所占的体积。符号为Vm。 ②Vm=,单位为L/mol。 ③特例:标准状况下的气体摩尔体积约为22.4 L/mol。 ④当温度、压强一定时,任何具有相同微粒数的气体都具有大致相同的体积。 ①物质的质量、摩尔质量、微粒个数不受“温度、压强”外界条件的影响。 ②使用“22.4 L/mol”时,一看是否为“标准状况”,二看是否为“气体”。 (4) 物质的量浓度 ①以单位体积溶液里所含溶质B的物质的量来表示溶液组成的物理量,叫作溶质B的物质的量浓度,符号为cB。单位:mol/L。 ②cB==。ρ的单位:g/cm3,w为质量分数,M的单位为g/mol。 1 钠及其化合物 (1) Na2O2常用作制氧剂、漂白剂 Na2O2由Na+和O构成;1 mol Na2O2反应转移1 mol电子。 (2) Na2CO3和NaHCO3的用途、转化及区别 ①用途 a. Na2CO3溶液浸泡废金属,除去金属表面的油污; b. NaHCO3用作食品疏松剂:2NaHCO3Na2CO3+H2O+CO2↑; c. 泡沫灭火器原理:6NaHCO3+Al2(SO4)3===3Na2SO4+2Al(OH)3↓+6CO2↑。 ②转化:Na2CO3NaHCO3 ③向NaOH溶液中通入CO2: 少量CO2:2NaOH+CO2===Na2CO3+H2O 足量CO2:NaOH+CO2===NaHCO3 ④鉴别: 性质 操作 结论 说明 稳定性 取等质量的两种固体,分别加热 生成能使澄清石灰水变浑浊气体的是NaHCO3 不能用Ca(OH)2[或Ba(OH)2或BaCl2或CaCl2]溶液鉴别Na2CO3和NaHCO3,因为都有白色沉淀生成,现象相同,无法鉴别 碱性 取等物质的量的两种固体,加入等体积(足量)水,测定pH 碱性强的是Na2CO3 与酸反应速率 取等体积、等物质的量浓度的两种盐溶液,分别逐滴加入等浓度的盐酸 产生气泡较快的是NaHCO3 (3) 侯氏制碱法 生产流程可简要表示如下: ①先在低温的条件下将NH3通入饱和食盐水中(要防倒吸),再通入CO2。 ... ...
~~ 已预览到文档结尾了 ~~