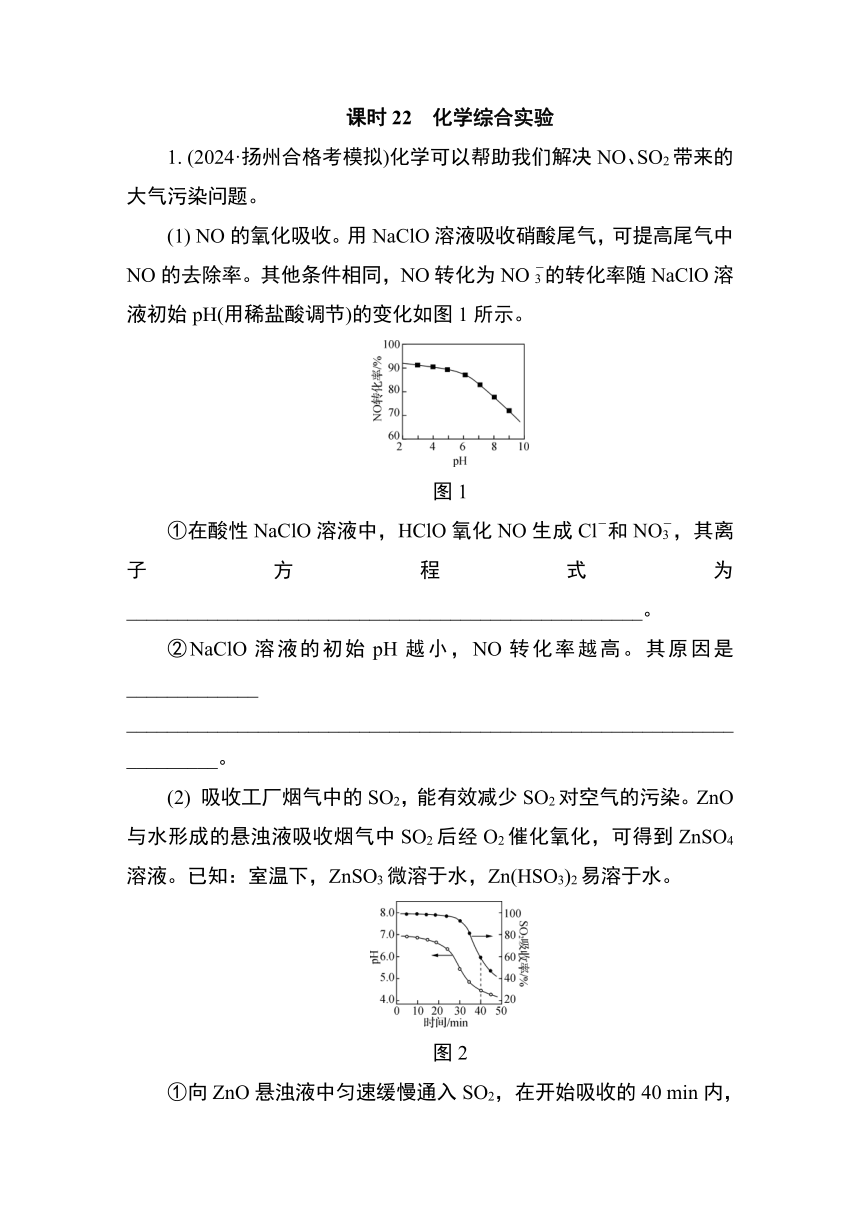

课时22 化学综合实验 1. (2024·扬州合格考模拟)化学可以帮助我们解决NO、SO2带来的大气污染问题。 (1) NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为NO的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图1所示。 图1 ①在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO,其离子方程式为_____。 ②NaClO溶液的初始pH越小,NO转化率越高。其原因是_____ _____。 (2) 吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。ZnO与水形成的悬浊液吸收烟气中SO2后经O2催化氧化,可得到ZnSO4溶液。已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水。 图2 ①向ZnO悬浊液中匀速缓慢通入SO2,在开始吸收的40 min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化,如图2所示。0~20 min溶液pH几乎不变的主要原因是_____。 ②测定某ZnSO4溶液的浓度。准确量取2.50 mL该 ZnSO4溶液于100 mL容量瓶中,加水稀释至刻度;准确量取20.00 mL稀释后的溶液于锥形瓶中,滴加氨水调节溶液pH=10,用0.015 0 mol/L EDTA(Na2H2Y)溶液反应至终点(反应为Zn2++Y4-===ZnY2-),并重复3次,平均消耗EDTA溶液25.00 mL。计算该ZnSO4溶液的物质的量浓度(写出计算过程)。 2. (2024·盐城合格考模拟)亚硝酸钠(NaNO2)是一种白色结晶状粉末,易溶于水,易被氧化,可用作织物染色的媒染剂、漂白剂等;工业制取亚硝酸钠晶体的基本流程如图所示。现设计相关实验测定其产品纯度。 (1) 吸收:Na2CO3溶液从设备顶部以雾状喷下吸收从底部通入的尾气,其优点是_____。 (2) 还原:若硝酸在“还原”阶段只生成NO2,则氧化剂与还原剂的物质的量之比为_____。 (3) 测定产品中NaNO2纯度。实验操作如下: ⅰ. 用电子天平称取7.500 g样品,配成500 mL样品溶液。 ⅱ. 向锥形瓶中准确移入50.00 mL样品溶液,滴加适量的H2SO4溶液酸化,加热至40~50 ℃,冷却后,用0.10 mol/L酸性KMnO4溶液进行滴定(已知:2MnO+5NO+6H+===2Mn2++5NO+3H2O),至恰好完全反应,消耗KMnO4溶液40.00 mL。 ⅲ. 重复滴定三次。 ①测定时操作时间不宜过长,否则测定的结果将会_____(填“偏大”或“偏小”)。 ②该亚硝酸钠晶体产品中可能含有的杂质有:_____、Na2CO3和NaHCO3。 ③试计算产品中NaNO2纯度(即NaNO2的质量分数)(写出计算过程)。 3. (2023·镇江句容学测合格考)ClO2是一种易溶于水的黄绿色气体,可用作安全高效的水处理剂,制备ClO2并被吸收的原理及装置如下: 已知装置A中发生的反应: 2NaClO3+4HCl===2ClO2↑+Cl2↑+2H2O+2NaCl(主反应) NaClO3+6HCl===NaCl+3Cl2↑+3H2O(副反应) (1) 装置B中发生的主要反应的化学方程式为_____。 (2) 实验过程中不断缓慢通入N2的目的是_____。 (3) 单位体积ClO2吸收液中含有ClO2的质量的实验测定步骤如下。 步骤1:配制Na2S2O3溶液。准确称取1.984 0 g Na2S2O3·5H2O,用新煮沸并冷却的蒸馏水配成100.0 mL溶液。 步骤2:准确移取1.00 mL装置C中的吸收液加入锥形瓶中,加入丙二酸静置后,再加入适量硫酸及稍过量的KI溶液(2ClO2+10I-+8H+===5I2+2Cl-+4H2O),在暗处放置5 min。 步骤3:向步骤2的锥形瓶的反应液中加入1 mL淀粉溶液作指示剂,再向其中滴加步骤1配制的Na2S2O3溶液(发生反应I2+2Na2S2O3===2NaI+Na2S4O6),至恰好完全反应时消耗Na2S2O3溶液20.00 mL。 ①配制Na2S2O3溶液时,蒸馏水需煮沸的原因是_____。 ②计算装置C中,每1.00 mL ClO2吸收液中含有ClO2的质量(单位:mg)(写出计算过程)。 课时22 化学综合实验 1. (1) ①3HClO+2NO+H2O ===3Cl-+2NO+5H+ ②溶液pH越小,溶液中HClO的浓度越大,氧化NO的能力越强 (2) ①此时主要是ZnO与SO2反应生成ZnSO3 ②由题意得关系式:Zn2+ ... ...
~~ 已预览到文档结尾了 ~~