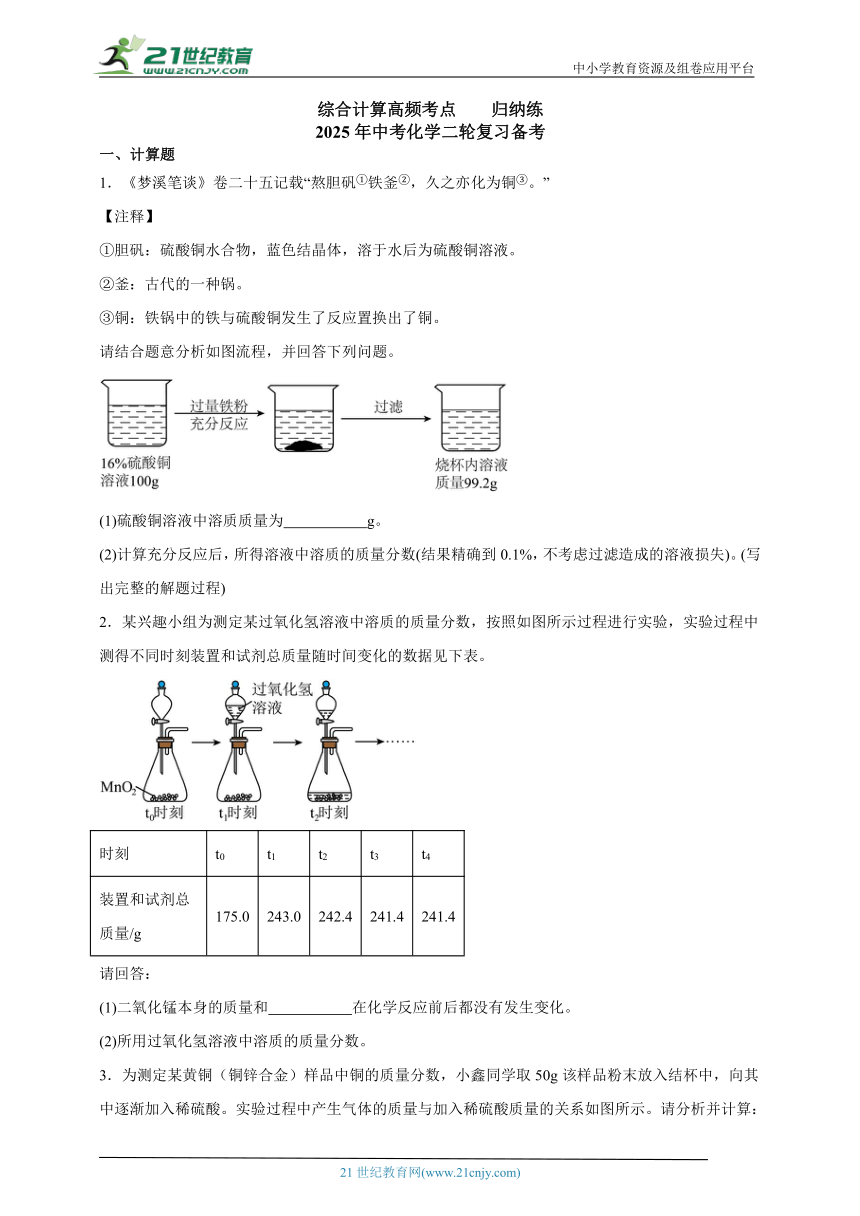

中小学教育资源及组卷应用平台 综合计算高频考点 归纳练 2025年中考化学二轮复习备考 一、计算题 1.《梦溪笔谈》卷二十五记载“熬胆矾①铁釜②,久之亦化为铜③。” 【注释】 ①胆矾:硫酸铜水合物,蓝色结晶体,溶于水后为硫酸铜溶液。 ②釜:古代的一种锅。 ③铜:铁锅中的铁与硫酸铜发生了反应置换出了铜。 请结合题意分析如图流程,并回答下列问题。 (1)硫酸铜溶液中溶质质量为 g。 (2)计算充分反应后,所得溶液中溶质的质量分数(结果精确到0.1%,不考虑过滤造成的溶液损失)。(写出完整的解题过程) 2.某兴趣小组为测定某过氧化氢溶液中溶质的质量分数,按照如图所示过程进行实验,实验过程中测得不同时刻装置和试剂总质量随时间变化的数据见下表。 时刻 t0 t1 t2 t3 t4 装置和试剂总质量/g 175.0 243.0 242.4 241.4 241.4 请回答: (1)二氧化锰本身的质量和 在化学反应前后都没有发生变化。 (2)所用过氧化氢溶液中溶质的质量分数。 3.为测定某黄铜(铜锌合金)样品中铜的质量分数,小鑫同学取50g该样品粉末放入结杯中,向其中逐渐加入稀硫酸。实验过程中产生气体的质量与加入稀硫酸质量的关系如图所示。请分析并计算: (1)生成氢气的总质量是 。 (2)根据题目信息, (填“可以”或“不能”)算出用稀硫酸的溶质质量分数。 (3)计算该黄铜样品中铜的质量分数。 4.现有氯化钙和氯化钠的固体混合物,进行如下实验: 请计算: (1)反应生成沉淀的质量是 g。 (2)所用碳酸钠溶液的溶质质量分数。 5.向盛有40g氢氧化钠溶液的锥形瓶中逐滴滴加100g溶质质量分数为4.9%的稀硫酸,用pH传感器测得溶液的pH变化情况如图所示。 (1)A点对应的溶液中溶质有 种。 (2)发生反应的化学方程式为 。 (3)氢氧化钠溶液中溶质的质量分数为 。 (4)用98%的浓硫酸配制上述稀硫酸,需加水的质量为 。 6.小明用石灰石测定某稀盐酸中溶质的质量分数,进行了如图甲所示的实验。随着实验的进行烧杯内物质的质量变化如图乙所示。请计算: (1)产生二氧化碳的总质量为 g。 (2)稀盐酸中溶质的质量分数。 7.某兴趣小组设计图1实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图2。 提示: ①醋酸和碳酸钙反应的化学方程式为CaCO3 + 2HAc=CaAc2 +H2O+CO2↑。 ②鱼骨中其他成分与食醋反应生成的气体可忽略不计。 (1)该实验中浓硫酸的作用是 。 (2)若用50g溶质质量分数为9%的醋酸溶液配制150g溶质质量分数为3%的醋酸溶液,需要加水 g。 (3)根据图中的数据计算鱼骨中碳酸钙的质量分数(无计算过程不得分)。 (4)生活中,用喝醋的方法除去卡在咽上的鱼刺,这种做法 (填“是”或“不是”)科学的。请你结合图中数据加以说明: 。 8.某实验小组为测定某过氧化氢溶液的溶质质量分数,进行了过氧化氢溶液的分解实验,实验中记录的相关数据如下表。 反应前物质的质量 完全反应后物质的质量 过氧化氢溶液质量 二氧化锰质量 固体与液体混合物质量 氧气质量 68.0g _____g 66.6g 1.6g 请回答: (1)二氧化锰由 种元素组成,其质量为 g。 (2)该过氧化氢溶液的溶质质量分数(写出完整的计算过程)。 9.黄铜被广泛用于制作机器零件、日用品等。当锌的质量分数小于39%时,黄铜的塑性好,适于冷热加压加工。为了解某黄铜样品的性能进行如下实验:取20g该样品于烧杯中,另取60g稀硫酸,分3次加入,每次均充分反应,测定实验数据如表。 实验次数 第1次 第2次 第3次 加入稀硫酸的质量/g 20 20 20 生成氢气的质量/g 0.08 ? 0.04 请完成下列分析及计算: (1)第2次生成氢气的质量为 g。 (2)通过计算判断该黄铜是否适于冷热加压加工。 10.为测定一瓶标签破损(如图)的钙片中碳酸钙的含量,某同学做了如下实验:取 20 片钙片,放入干燥、洁净的烧杯中,然后逐滴滴加稀盐酸,当加 ... ...
~~ 已预览到文档结尾了 ~~